Ein besonderer Fall von Qualität: Sichere Prozesse rund um Ihre Medizinprodukte
Software für Qualitätsmanagement nach DIN EN ISO 13485
- Alle Abläufe nach ISO 13485 managen
- Methodische Grundlagen umsetzen
- Zertifizierungskonform arbeiten

Vertrieb & Kundenbetreuung Kontakt zu Marion

Beratung & Support Kontakt zu Kay
Hersteller von Medizinprodukten müssen besonderes Augenmerk auf die Sicherheit von Patienten und Anwendern legen. Um diese Sicherheit zu gewährleisten, ist das Qualitätsmanagement entscheidend. Grundlage ist die europäische Medizinprodukteverordnung (Medical Device Regulation). Die Medical Device Regulation (MDR) tritt mit dem 26. Mai 2021 in Kraft. Viele Hersteller von Medizinprodukten müssen damit in kurzer Zeit eine Zertifizierung erlangen. Ein Unterschied der MDR gegenüber der bisherigen MDD 93/42 EWG ist, dass sie als Verordnung allgemeine Gültigkeit und unmittelbare Wirksamkeit in allen EU-Mitgliedstaaten hat. Das soll zu einer einheitlichen Regelung für das Inverkehrbringen von Medizinprodukten führen. Ein stärkerer Fokus liegt dabei auf Produktqualität und -sicherheit.
Die Änderungen betreffen:
- Klassifizierung der Medizinprodukte
- Konformitätsbewertungsverfahren
- Technische Dokumentation
- Klinische Bewertung / Prüfungen
- Verantwortliche Person
- Marktüberwachung
- Meldepflichten
- Transparenz
- Qualitätsmanagement
Qualitätsmanagement und Medizinprodukte-Anforderungen unter einem Dach
- Branchenspezifische Anforderungen
- Kontinuierliche Verbesserung
- Durchgehende Dokumentation
Wenn Sie medizinische Produkte in kontinuierlich bester Qualität entwickeln, herstellen und vertreiben, müssen Sie hohe Ansprüche erfüllen. Da ist ein Qualitätsmanagement gefragt, dass über den Standard der ISO 9001 hinausgeht. Die ISO 13485 ist genau dieser erweiterte Rahmen, mit dem Sie durch sichere Prozesse Ihre Abläufe steuern und Dokumente lenken. Die ISO 13485 ist die branchenspezifisch erweiterte Variante der Qualitätsnorm ISO 9001:2008. Mit diesem Regelwerk erstellen Sie ein interaktives Qualitätsmanagementsystem, welches das Informationsportal Ihres Unternehmens ist. Allen Beteiligten werden schnell und effektiv relevante und aktuelle Daten zur Verfügung gestellt.
Gut vorbereitet für Audits und Zertifizierung
Bauen Sie mit orgavision ein digitales Qualitätsmanagementsystem auf, das Ihre Abläufe korrekt abbildet und die Dokumente normkonform und durchgehend steuert. Gleichzeitig führen Audits, Managementbewertungen und das Feedback von Kunden und Mitarbeitern zu einer kontinuierlichen Verbesserung – und Sie dokumentieren alles an einer Stelle. So sind auch Ihre Mitarbeitenden immer gut vorbereitet und Informationen sind aktuell und jederzeit verfügbar.
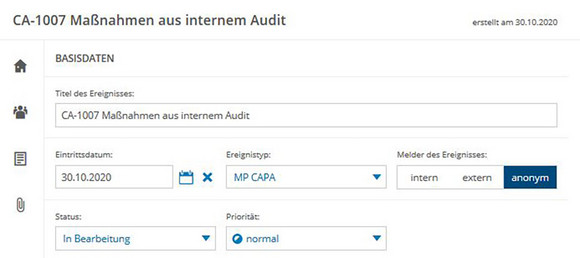
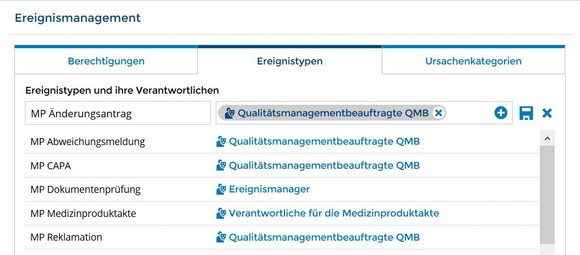
Ereignisse im Produktionsprozess erfassen
Mithilfe des Ereignismanagement-Moduls erfassen Sie Ereignisse wie Beinahe-Unfälle, Fehler oder Reklamationen und weisen diesen explizite Ursachen zu. Auswertungen der Ereignisse geben Ihnen einen genauen Überblick, an welchen Stellen Verbesserungspotential besteht oder welche Prozesse Risiken bergen. Das Ereignismanagement-Modul bindet alle Beteiligten interaktiv in die CAPA-Prozesse, Änderungsverfolgung oder Reklamationsmanagement ein und macht die Abläufe noch effektiver. Und alles ist sofort für spätere Überprüfungen sicher dokumentiert.